List of thumbnails
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
lumeneinheit und die auf ein Molekül infolge des Konzentrations-
gefälles wirkende
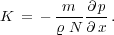 | (2) |
Ist die Lösung genügend verdünnt, so ist der osmotische
Druck durch die Gleichung
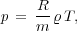 | (3) |
wobei T die absolute Temperatur und R = 8,31.107 ist. Aus
den Gleichungen (1), (2) und (3) erhalten wir für die Ge-
schwindigkeit der Wanderung der gelösten
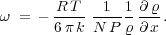
Die pro Zeiteinheit durch die Einheit des Querschnittes
in Richtung der X - Achse hindurchtretende Stoffmenge ist
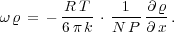 | (4) |
Wir erhalten also für den Diffusionskoeffizienten D
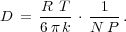
Man kann also aus dem Diffusionskoeffizienten und dem
Koeffizienten der inneren Reibung des Lösungsmittels das Pro-
dukt aus der Anzahl N der wirklichen Moleküle in einem
Grammolekül und dem hydrodynamisch wirksamen Molekular-
radius P
In dieser Ableitung ist der osmotische Druck wie eine
auf die einzelnen Moleküle wirkende Kraft behandelt worden,
was offenbar der Auffassung der kinetischen Molekulartheorie
nicht entspricht, da gemäß letzterer in dem vorliegenden Falle
der osmotische Druck nur als eine scheinbare Kraft aufzu-
fassen ist. Diese Schwierigkeit verschwindet jedoch, wenn man
bedenkt, daß den (scheinbaren) osmotischen Kräften, welche
den Konzentrationsverschiedenheiten der Lösung entsprechen,
durch ihnen numerisch gleiche, entgegengesetzt gerichtete, auf
die einzelnen Moleküle wirkende Kräfte das (dynamische) Gleich-