| Scan | Original |
|---|---|
| 1 | |
| 2 | |
| 3 | |
| 4 | |
| 5 | |
| 6 | |
| 7 | |
| 8 | |
| 9 |
im Sinne des Chemikers (Äquivalentgewicht bezogen auf 1 g
Wasserstoff als Einheit) enthalten
Liege nämlich eine solche Quantität eines idealen Gases
vor, so ist bekanntlich, wenn Gramm und Zentimeter als Ein-
heiten benutzt
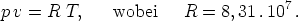
Nach der kinetischen Gastheorie ist
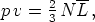
wobei L den Mittelwert der lebendigen Kraft der Schwerpunkts-
bewegung eines Moleküles bedeutet. Berücksichtigt man
noch,
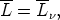
so erhält
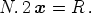
Die Konstante 2 x ist also gleich dem Quotienten der Kon-
stanten R in Anzahl der in einem Äquivalent enthaltenen
Setzt man mit O. E. Meyer N = 6, 4 . 1023, so erhält
man x = 6, 5 . 10-17.
§ 4. Allgemeine Bedeutung der Konstanten x.
Ein gegebenes System berühre ein System von relativ
unendlich großer Energie und der Temperatur T. Die Wahr-
scheinlichkeit dW dafür, daß der Wert seiner Energie in einem
beliebig herausgegriffenen Zeitpunkte zwischen E und E + dE
liegt,
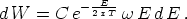
Für den Mittelwert 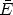 von E erhält
von E erhält
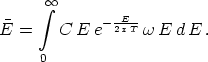
Da